1
Infografía nuevo biosimilar
Primer biosimilar de ranibizumab autorizado en Europa
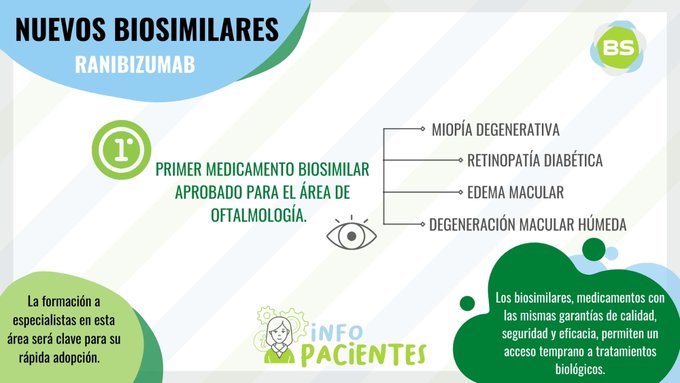 Tras recibir la opinión positiva del Comité de Medicamentos de Uso Humano (CHMP, siglas en inglés) de la Agencia Europea del Medicamento el 25 de junio de 2021, la Comisión Europea emitió una autorización de comercialización del primer biosimilar de ranibizumab el pasado 18 de agosto; Este es el primer biosimilar autorizado para el área de la Oftalmología. Ranibizumab está indicado en degeneración macular asociada a la edad, edema macular, retinopatía diabética y miopía degenerativa. Se abre así una oportunidad de acceso para los pacientes y también un reto para la formación de estos especialistas acerca de las garantías de seguridad, calidad y eficacia y otras cuestiones que ofrecen los medicamentos biosimilares.
Tras recibir la opinión positiva del Comité de Medicamentos de Uso Humano (CHMP, siglas en inglés) de la Agencia Europea del Medicamento el 25 de junio de 2021, la Comisión Europea emitió una autorización de comercialización del primer biosimilar de ranibizumab el pasado 18 de agosto; Este es el primer biosimilar autorizado para el área de la Oftalmología. Ranibizumab está indicado en degeneración macular asociada a la edad, edema macular, retinopatía diabética y miopía degenerativa. Se abre así una oportunidad de acceso para los pacientes y también un reto para la formación de estos especialistas acerca de las garantías de seguridad, calidad y eficacia y otras cuestiones que ofrecen los medicamentos biosimilares.
https://twitter.com/BioSim_es/status/1434894565408968712/photo/1
2
Artículo científico
Evaluación del uso de biosimilares de antiTNF para psoriasis en Reino Unido: un estudio del registro de biológicos e inmunomoduladores de la Asociación Británica de Dermatólogos
La Asociación Británica de Dermatólogos (BADBIR) ha lanzado una convocatoria para la realización de un estudio farmacoepidemiológico para evaluar el uso de biosimilares de anti-TNF (adalimumab, etanercept e infliximab) en el Reino Unido para el tratamiento de la psoriasis. Su objetivo es identificar la distribución y la penetración de biosimilares de anti-TNF en este país a lo largo del tiempo y comparar la efectividad y seguridad de estos con su original.
The University of Manchester, Faculty of Biology, Medicine and Health
3
Artículo científico
Evolución de los requisitos clínicos de los biosimilares: un estudio de entrevistas cualitativas con expertos de la industria y reguladores de las agencias nacionales del medicamento de Europa
En un estudio de entrevista cualitativa realizado a expertos de la industria y reguladores de la EMA estos valoran la posibilidad de que los requisitos de los ensayos de comparabilidad clínica de biosimilares cambien en un futuro próximo. Para ello se necesitaría claridad sobre cómo garantizar una correlación adecuada entre los datos fisicoquímicos, los estudios PK/PD y el efecto de los medicamentos en clínica, así como la manera de mantener una evaluación de inmunogenicidad suficiente. Conseguir tal claridad puede facilitar la evaluación reglamentaria de los próximos biosimilares.
Druedahl, L. C. et al. Evolving Biosimilar Clinical Requirements: A Qualitative Interview Study with Industry Experts and European National Medicines Agency Regulators. 2021. BioDrugs
https://pubmed.ncbi.nlm.nih.gov/33830478/
4
Artículo científico
Licitación de biológicos y biosimilares en Europa: una propuesta hacia prácticas más sostenibles
 Este trabajo de MABEL Fund emite recomendaciones para una adquisición sostenible para compradores y suministradores de biosimilares y sus originales en Europa. Se basa en una revisión del entorno europeo, donde estos medicamentos son adquiridos mayoritariamente por concurso público, y en los resultados de una encuesta a 60 farmacéuticos de hospital. Destacan en este trabajo la propuesta de concursos multiadjudicatario así como una serie de criterios adicionales al precio a incluir en las licitaciones. Sus recomendaciones globales se basan en i) transparencia e igualdad, ii) encontrar el momento idóneo para licitar, iii) cumplimiento de la legislación sobre contratación pública, iv) eficiencia, planificación y suministro a tiempo y v) competencia sostenible a largo plazo.
Este trabajo de MABEL Fund emite recomendaciones para una adquisición sostenible para compradores y suministradores de biosimilares y sus originales en Europa. Se basa en una revisión del entorno europeo, donde estos medicamentos son adquiridos mayoritariamente por concurso público, y en los resultados de una encuesta a 60 farmacéuticos de hospital. Destacan en este trabajo la propuesta de concursos multiadjudicatario así como una serie de criterios adicionales al precio a incluir en las licitaciones. Sus recomendaciones globales se basan en i) transparencia e igualdad, ii) encontrar el momento idóneo para licitar, iii) cumplimiento de la legislación sobre contratación pública, iv) eficiencia, planificación y suministro a tiempo y v) competencia sostenible a largo plazo.
Barbier, L. et al. Off-Patent Biologicals and Biosimilars Tendering in Europe-A Proposal towards More Sustainable Practices. 2021. Pharmaceuticals
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8225063/
5
Artículo científico
Consideraciones prácticas para integrar los biosimilares en la práctica clínica
 El desarrollo de productos biológicos innovadores y ahora de sus biosimilares ha creado algunos desafíos únicos en la práctica de la oncología. Un estudio a oncólogos clínicos formados en biosimilares pone de manifiesto que estos profesionales son imprescindibles en el éxito de la integración de estos fármacos en la práctica de la oncología. Para ello, es esencial el conocimiento sobre los biosimilares que se traduzca en mensajes veraces y rigurosos sobre estos a sus compañeros y a pacientes oncológicos; el análisis objetivo de datos comparativos entre cada producto biosimilar y el producto de referencia en términos de eficacia, seguridad, administración y consideraciones de precios y la educación adecuada a los pacientes sobre los beneficios y riesgos de utilizar productos biosimilares en su tratamiento contra el cáncer acompañada de materiales educativos desarrollados por estos profesionales a un nivel de grado apropiado para el alumno.
El desarrollo de productos biológicos innovadores y ahora de sus biosimilares ha creado algunos desafíos únicos en la práctica de la oncología. Un estudio a oncólogos clínicos formados en biosimilares pone de manifiesto que estos profesionales son imprescindibles en el éxito de la integración de estos fármacos en la práctica de la oncología. Para ello, es esencial el conocimiento sobre los biosimilares que se traduzca en mensajes veraces y rigurosos sobre estos a sus compañeros y a pacientes oncológicos; el análisis objetivo de datos comparativos entre cada producto biosimilar y el producto de referencia en términos de eficacia, seguridad, administración y consideraciones de precios y la educación adecuada a los pacientes sobre los beneficios y riesgos de utilizar productos biosimilares en su tratamiento contra el cáncer acompañada de materiales educativos desarrollados por estos profesionales a un nivel de grado apropiado para el alumno.
